Introducción
La espermatogénesis es un proceso fisiológico que implica la síntesis y diferenciación de los espermatozoides en el testículo (Griswold, 2016; Griswold & Hogarth, 2018). Este proceso se caracteriza por la proliferación de las espermatogonias por mitosis; la división de los espermatocitos genera células haploides por meiosis y la diferenciación morfológica de las espermátidas en los espermatozoides (Griswold, 2016; Holt, Stanger, Nixon & McLaughlin, 2016; Ni, Hao & Yang, 2019). Posteriormente, los espermatozoides son liberados al lumen de los túbulos seminíferos para ser transportados a través de los conductos eferentes hasta el epidídimo (Griswold, 2016). Durante su tránsito por el epidídimo, los espermatozoides presentan modificaciones bioquímicas, morfológicas y fisiológicas que favorecen el potencial fecundante de los gametos (Gervasi & Visconti, 2017). Sin embargo, los espermatozoides eyaculados aún no son capaces de fecundar un ovocito; esta capacidad se adquiere durante el tránsito por el tracto reproductor femenino, en el que ocurren una serie de cambios bioquímicos y fisiológicos, descritos como capacitación espermática (Austin, 1952; Chang, 1951). Es en el tracto en donde el espermatozoide desarrolla una movilidad hiperactiva (patrón de movilidad asimétrica, es decir, fuerte batido flagelar asimétrico de alta amplitud y baja frecuencia), proceso que se requiere para liberar al espermatozoide adherido al epitelio del oviducto (Gervasi & Visconti, 2016; Stival et al., 2016; Suarez & Ho, 2003) . Finalmente, después de la capacitación, ocurre la liberación de las enzimas proteolíticas contenidas en el acrosoma de los gametos [la reacción acrosómica (RA)]; evento que se cree que es desencadenado por la unión del espermatozoide a la zona pelúcida (ZP) del ovocito (Buffone, 2016). Sin embargo, ahora se sabe que la RA ocurre por estimulación de moléculas sintetizadas por las células del cúmulo antes de llegar a la ZP (Hirohashi, Gerton & Buffone, 2011; Jin et al., 2011; Okabe, 2016).
Los procesos fisiológicos que ocurren en los espermatozoides como la hiperactivación, la capacitación y la RA, están relacionados con el cambio en la concentración de calcio intracelular ([Ca2+]i). En los mamíferos, se ha descrito que el aumento de [Ca2+]i se debe a su liberación desde depósitos internos como el acrosoma y la envoltura nuclear redundante (ENR), y a su captación desde el medio extracelular a través de canales iónicos y transportadores presentes en la membrana plasmática y en la membrana de los depósitos internos (Costello et al., 2009; Jin & Yang, 2017). Exclusivamente en los espermatozoides se ha descrito el canal de cationes implicado en el transporte de Ca2+, conocido como CatSper, que es uno de los principales canales involucrados en el incremento de [Ca2+]i (Brown et al., 2017). La actividad de este canal se ha asociado con la fertilidad masculina al regular procesos fisiológicos como la hiperactivación dependiente de [Ca2+]i en humanos y en ratones, así como la quimiotaxis en los erizos de mar. Sin embargo, la participación de CatSper en la RA aún no está clara.
Este canal se encuentra en la membrana plasmática de la pieza principal del flagelo y fue identificado en espermatozoides de ratón en el año 2001 mediante la clonación de su gen (Ren et al., 2001). CatSper contiene el mayor número de subunidades en comparación con cualquier canal iónico conocido (Lin, Ke, Zhang, Yan & Wu, 2021). Se ha reportado que los defectos en el gen que codifica CatSper o cualquiera de sus subunidades alteran la hiperactivación del espermatozoide, lo que impide su llegada al ovocito, la penetración a través de las células circundantes y la fertilización, impactando negativamente en la fertilidad masculina (Chung, Navarro, Krapivinsky & Clapham, 2011; Liu, Xia, Cho, Clapham & Ren, 2007; Qi et al., 2007; Singh & Rajender, 2015; Wang, Liu, Cho & Ren, 2009). Además, para aclarar la participación de CatSper en la fisiología espermática, se han realizado estudios generando modelos knockout para: anticuerpos específicos (Singh & Rajender, 2015; Ren et al., 2001), inhibidores de canales de Ca2+ (Lishko, Botchkina & Kirichok, 2011; Strünker et al., 2011) y patch-clamp (Lishko et al., 2011; Strünker et al., 2011). En esta revisión abordaremos la estructura, funciones, mecanismos de activación y conservación filogenética de CatSper.
CatSper
Estructura de CatSper
El canal CatSper está formado por al menos 10 subunidades que en conjunto forman un complejo heteromérico (Lin et al., 2021; Rahban & Nef, 2020). Tiene cuatro subunidades alfa (α), (CatSper1-4) que participan en la formación de poros y seis subunidades auxiliares CatSper beta (β), CatSper delta (δ), CatSper gamma (γ), CatSper épsilon (Ɛ), CatSper zeta (ζ) y EFCAB9 (proteína similar a la calmodulina que actúa como sensor dual del Ca2+ y del pH), ubicadas en la membrana plasmática de la pieza principal del flagelo (Figura 1), (Chung et al., 2017; Darszon, Nishigaki, Beltrám & Treviño, 2011; Rahban & Nef, 2020). Además, se han identificado proteínas adicionales a este complejo: C2CD6, (CatSper τ), (Yang et al., 2021), SLCO6C1 y TEM249 (Lin et al., 2021).
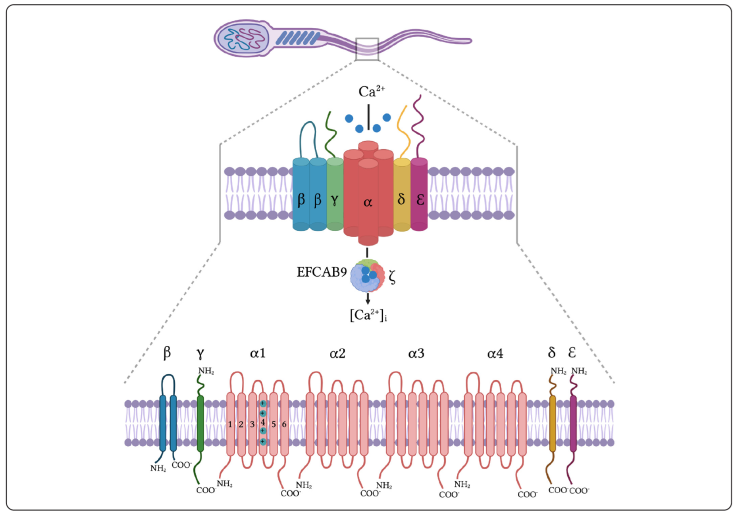
Figura 1 CatSper. El canal, ubicado en la pieza principal del flagelo del espermatozoide, forma un complejo heteromérico que consta de cuatro subunidades α que forman un poro y seis subunidades auxiliares: CatSper β (beta), CatSper δ (delta), CatSper γ (gamma), CatSper Ɛ (épsilon), CatSper ζ (zeta); y EFCAB9 (proteína similar a la calmodulina que actúa como un sensor dual para Ca2+ y pH). Cada subunidad α está formada por seis segmentos transmembrana (S1-6), de los cuales S4 detecta el voltaje a través de los aminoácidos cargados positivamente (lisina/arginina) y S5-6 forman el poro del canal (Rahban & Nef, 2020).
Mediante microscopía de alta resolución, observaron que el canal CatSper forma cuatro compartimentos lineales en la membrana flagelar, lo que forma un nanodominio de señalización en los cuadrantes flagelares. La importancia de la organización de los nanodominios flagelares es esencial para regular el movimiento ondulatorio del batido flagelar y, por tanto, la movilidad espermática (Zhao et al., 2021). La estructura y distribución de las subunidades de CatSper son esenciales para el funcionamiento del canal (Qi et al., 2007). Los estudios sobre este concluyen que la ausencia del canal iónico o la deficiencia de alguna de sus subunidades afecta a la fertilidad masculina, impidiendo que el espermatozoide llegue a la zona de reconocimiento con el ovocito y lo fecunde (Pereira, Sá, Barros & Sousa, 2017).
CatSper α
La primera estructura de CatSper que identificaron fue la de las subunidades α, CatSper1, mediante la clonación putativa del gen que codifica a la subunidad (Ren et al., 2001). CatSper1 es diferente de las otras tres subunidades α (CatSper2-CatSper4), ya que tiene un dominio terminal citoplasmático rico en histidinas que funciona como un sensor de pH (alcalinización), [83 histidinas en 446 aminoácidos que componen el amino-terminal (N-terminal)], (Ren et al., 2001; Chung et al., 2011; Darszon et al., 2011; Lin et al. , 2021). Además, un conjunto de estudios realizados por Ren et al. (2001) la localizaron en el espermatozoide y atribuyeron a CatSper como una proteína necesaria para la movilidad normal de los gametos masculinos y su penetración en la ZP que rodea al ovocito. En el mismo año, CatSper2 fue identificada en un espermatozoide de ratón, de rata y de humano, mostrando un 21% de homología y un 40% de similitud de la región transmembranal al compararla con CatSper1 (Quill, Ren, Clapham & Garbers, 2001). Así mismo, Lobley, Pierron, Reynolds, Allen & Michalovich (2003), mediante identificación génica in silico, obtuvieron las secuencias de CatSper3 y CatSper4 en ratones y en humanos. Además, describieron dominios de interacción proteína -proteína en el grupo carboxilo terminal (C-terminal) de cada una de las subunidades α de CatSper y sugerir que CatSper1-4 interactúa directa o indirectamente para formar un tetrámero funcional (Lobley et al., 2003; Babcock, 2007). Al igual que con CatSper 1 y 2, se demostraron que las subunidades CatSper3 y 4 se localizan en la pieza principal del flagelo y que la alteración genética de cualquiera de las cuatro subunidades afecta a los espermatozoides al modificar la actividad del canal CatSper, lo que, conduce a la pérdida de la movilidad hiperactivada (Quill et al., 2001; Quill, Sugden, Rossi, Doolittle, Hamer & Garbers, 2003; Qi et al., 2007). Cada subunidad α tiene seis segmentos transmembranales (TMS); los primeros cuatro TMS (S1-4) contienen un sensor de voltaje y los dos últimos (S5 y S6) unidos por una estructura cíclica hidrofóbica forman el poro del canal (Figura 1), (Lin et al., 2021; Singh & Rajender, 2015). Cuatro residuos de glutamina/aspartato (Asp536, Asp295, Asp227 y Asp237) se repiten en la región del poro, lo que proporciona selectividad de Ca2+ en el canal (Singh & Rajende, 2015; Navarro, Kirichok, Chung & Clapham, 2008; Lin et al., 2021). Los S1-4 están unidos por una estructura cíclica corta, donde los aminoácidos con carga positiva (lisina/arginina) están presentes en la región transmembranal S4 para detectar el voltaje y activar el canal. La cantidad de residuos cargados positivamente en S4 varía según la subunidad α; siete en CatSper1, cuatro en CatSper2 y dos en CatSper3 (Lin et al., 2021).
Por otra parte, Ren y colaboradores determinaron que el ARNm y la proteína CatSper1-3 sólo están presentes en el testículo, diferente a CatSper4 que se expresa en los tejidos testicular, placentario y pulmonar (Ren et al., 2001). En el análisis de microarreglos encontraron: el ARNm de CatSper2 en los espermatocitos en la etapa de paquiteno a los 12 días posparto en testículos de ratón, y a CatSper1 en las espermátidas redondas el día 20 posparto (Schultz, Hamra & Garbers, 2003), así como a CatSper 3 y CatSper 4 (Jin, O`Doherty, Wang, Zheng, Sanders & Yan, 2005).
CatSper β
Tras identificar las cuatro proteínas (CatSper1-4) implicadas en el ensamblaje de CatSper, la primera subunidad auxiliar en ser identificada fue CatSper β, a partir de búsquedas en las bases de datos y uso del PCR de transcripción inversa (Liu et al., 2007). En ratón, CatSper β está formada por dos dominios transmembranales de 1,109 aminoácidos con un peso de 126 kDa; un dominio extracelular de (1,060-1,076 aminoácidos) y un dominio intracelular de (6-22 aminoácidos), (Lin et al., 2021). La expresión de ARNm se llevó a cabo en espermatocitos y espermátidas, pero no en espermatogonias (Liu et al., 2007).
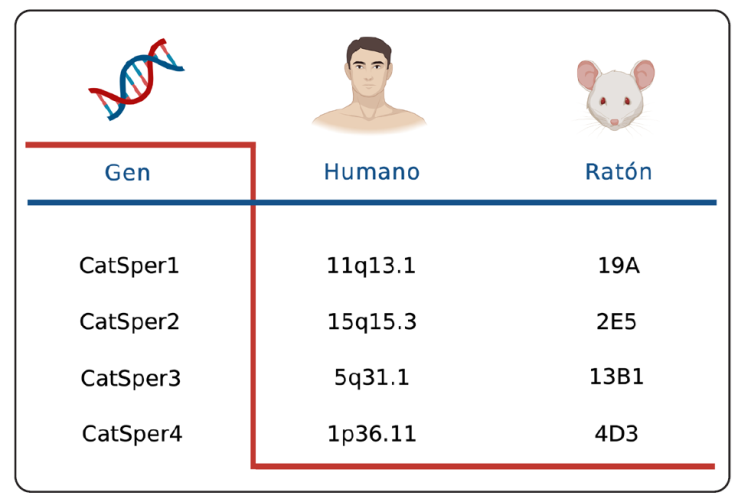
Modificado de: Singh & Rajender, 2015.
Figura 2 Localización genética de las subunidades CatSper α (1-4) en humanos y en ratones.
La búsqueda en las bases de datos indica que CatSper β es de función desconocida. Además, esta subunidad se conserva entre humanos y ratones con una identidad del 56 % (Liu et al., 2007).
CatSper γ
Wang et al. (2009) identificaron la segunda subunidad auxiliar, CatSper γ, en ratones con 1,145 aminoácidos y un peso molecular de 131 kDa. La estructura de CatSper γ se limita a un segmento transmembranal con un dominio extracelular de (1,000 aminoácidos) y un dominio intracelular de (58 aminoácidos). También detectaron ARNm en testículos, específicamente en los espermatocitos y en las espermátidas de ratón (Wang et al., 2009), como se describió para las subunidades α (Babcock, 2007) y β (Liu et al., 2007). CatSper γ en el espermatozoide se encuentra en la pieza principal (Wang et al., 2009). Cabe destacar que CatSper γ está presente en los genomas de animales en los que este se localiza, incluidos el de ratón, el de humanos y el de erizo de mar con un 55% de identidad entre el ser humano y el ratón (Wang et al., 2009). Sin embargo, está ausente en el genoma de animales como Drosophila melanogaster y Caenorhabditis elegans (Wang et al., 2009).
CatSper δ
Mediante un análisis proteómico de purificación por afinidad seguido de espectrometría de masas, se identificó que el gen Tmem146 codifica la subunidad auxiliar CatSper δ que tiene un supuesto dominio transmembranal (Lin et al., 2021). El ARNm de CatSperδ se detectó en espermatocitos y espermátidas en diferentes etapas de la espermatogénesis, como se encontró previamente para CatSpers1-4, CatSperβ y CatSperγ. CatSperδ tiene 805 aminoácidos de longitud con un peso molecular de 91 kDa. En el ratón, esta subunidad tiene un dominio extracelular de 699 aminoácidos seguido de un dominio transmembranal que termina en una cola intracelular de 60 aminoácidos (Chung et al., 2011).
Las subunidades α, β y γ de CatSper tienen el mismo patrón evolutivo; sus ortólogos están presentes en los genomas de mamíferos, así como en el de las ascidias (Ciona intestinalis) y en el de los erizos de mar (Strongylocentrotus purpuratus), (Cai & Clapham, 2008). Los ortólogos de CatSperδ los encontraron sólo en mamíferos y en un reptil (Anolis carolinensis), lo que implica que CatSperδ imparte una función específica de la especie y muestra signos de cambio evolutivo rápido debido a que la identidad de secuencia entre CatSperδ humano y de ratón es baja (51%), (Chung et al., 2011). CatSper δ es necesario para la estabilidad de la formación del complejo CatSper, ya que se encontró que la ausencia de esta subunidad en el ratón disminuye el flujo de Ca2+ y la movilidad hiperactivada (Chung et al., 2011).
CatSper Ɛ and ζ
En el año 2017, se dio a conocer que los genes Gm7068 y Tex40 codifican las subunidades transmembranales CatSper Ɛ y CatSper ζ, respectivamente. Al igual que las otras subunidades auxiliares de CatSper, los ARNm de CatSper Ɛ y CatSper ζ se expresan específicamente en las células germinales (Chung et al., 2017; Brown et al., 2018). Además, en el espermatozoide de humano y de ratón, estas proteínas se encuentran en la pieza principal del flagelo (Chung et al., 2017). A diferencia de CatSper Ɛ, la subunidad ζ no contiene dominios transmembranales, es un componente citoplasmático de CatSper (Chung et al., 2017), que se compone principalmente de hélices α.
CatSper Ɛ y CatSper ζ en humanos y ratones muestran un cambio evolutivo rápido con un 50% y 40% de identidad de secuencia de aminoácidos, respectivamente. Se demostró que CatSper ζ se conserva sólo en mamíferos, esto sugiere que la adaptación de esta proteína está involucrada en la reotaxis espermática dentro del tracto reproductivo femenino, ya que observaron que la alteración genética CatSper ζ reduce la corriente CatSper y la flexibilidad del flagelo afectando la movilidad hiperactivada y la reotaxis espermática, cuyo resultado es la subfertilidad. Es decir, los espermatozoides de ratones nulos CatSper ζ logran un 20% de fertilización (Chung et al., 2017).
Mediante un análisis bioinformático, determinaron una alta homología entre las subunidades CatSper Ɛ y CatSper δ (52% de aminoácidos idénticos/similares) al alinear las secuencias extracelulares de estas proteínas, lo que sugiere que CatSper Ɛ cumple la función de estabilizar el ensamblaje del complejo CatSper (Chung et al., 2017; Brown et al., 2018).
EFCAB9
En un análisis proteómico y genómico comparativo, identificaron la proteína 9 que contiene un dominio EF de unión a Ca2+ (EFCAB9), que modula la actividad y organización de CatSper (Hwang et al., 2019). Confirmaron que el gen Efcab9 se expresa sólo en el testículo y se conserva evolutivamente a partir de los eucariotas unicelulares flagelados como otras subunidades transmembranales de CatSper y está intracelularmente en el cuerpo principal del espermatozoide. A diferencia de las subunidades auxiliares descritas previamente, EFCAB9 tiene tres motivos de unión al Ca2+, que son las cadenas laterales de ácido aspártico y glutámico ubicadas en cada bucle (Hwang et al., 2019). Además, tiene dos cadenas que contienen el dominio EF, que es una proteína similar a la calmodulina (Hwang et al., 2019).
Estudios in vivo determinaron la función de la subunidad EFCAB9 a nivel molecular, celular, bioquímico y electrofisiológico. La describieron como un sensor de Ca2+ dependiente del pH, en enlace directo con la subunidad ζ de CatSper. Ambas subunidades activan el canal CatSper en respuesta a cambios en el pH intracelular y el Ca2+ en los espermatozoides (Hwang et al., 2019). La interacción que depende del Ca2+ entre EFCAB9 y CatSper ζ es necesaria para desarrollar una movilidad hiperactivada en los espermatozoides (Chung et al., 2017; Hwang et al., 2019). CatSper ζ en humanos y ratones contiene un motivo conservado esencial para la interacción con EFCAB9 (Hwang, Maziarz, Wagner & Chung, 2021).
La ausencia de EFCAB9, a pesar de la morfología y concentración de espermatozoides normales, tanto la tasa de fertilización como el tamaño de la camada en ratón fueron menores, lo que sugiere subfertilidad (Hwang et al., 2019). Además, la ausencia del complejo EFCAB9 - CatSper ζ afecta la disposición, alineación y longitud de los nanodominios del canal CatSper en la membrana flagelar (Zhao et al., 2021).
CatSper τ
Los estudios de Yang et al. (2021), identificaron la proteína C2CD6 (proteína 6 que contiene el dominio C2 dependiente del Ca2+) como una nueva subunidad del canal CatSper, codificada por un gen específico de los testículos. Investigaciones posteriores mencionan que C2CD6 fue nombrada como CatSper tau (τ), (Hwang, Wang, Lu, Ikawa & Chung, 2022). CatSper τ se localiza en la pieza principal del espermatozoide del ratón y del humano. A diferencia de las otras subunidades, CatSper τ está en niveles bajos de proteína en ausencia de otra subunidad formadora del complejo CatSper (EFCAB9). Sin embargo, la ausencia de CatSper τ disminuye la entrada de Ca2+ en los espermatozoides, lo que afecta su movilidad y la fertilidad masculina. Un análisis de la movilidad de los espermatozoides en ratones KO CatSper τ determinó una disminución en la velocidad de natación (velocidad curvilínea y velocidad de trayectoria promedio) y la amplitud de la cabeza, lo que demuestra una pérdida de la hiperactivación de los espermatozoides (Hwang et al., 2022).
La pérdida de CatSper τ afecta la orientación de los nanodominios de señalización del Ca2+ organizados en la membrana flagelar, ya que es responsable de regular la distribución lineal, cuadrilateral o continua de los complejos CatSper (Hwang et al., 2022; Zhao et al., 2021). En las células germinales esta subunidad se dirige al complejo CatSper ensamblado en las espermátidas tempranas y a través de vesículas portadoras de canales se dirige al flagelo de las espermátidas tardías. Es decir, CatSper τ, regula la localización flagelar de CatSper y es indispensable para formar el complejo de canales a partir de los testículos (Hwang et al., 2022; Yang et al., 2021).
SLCO6C1 y TMEM249
SLCO6C1 es una proteína transportadora de aniones altamente expresada en el testículo. Fue identificada mediante microscopía crioelectrónica en espermatozoides de ratón (Lin et al., 2021) y localizada en la pieza principal del flagelo mediante microscopía de fluorescencia e iluminación estructurada 3D (Zhao et al., 2021). SLCO6C1 contiene un dominio N, C y Kazal (característico de los inhibidores de la serina proteasa). Además, se identificó un sitio de glicosilación (conservado en ratón, rata y humano) que está asociado con una interacción hidrofóbica con la subunidad CatSper Ɛ (Lin et al., 2021).
Lin et al. (2021) identificaron a la proteína TMEM249 en la pieza principal del flagelo mediante microscopía electrónica. Huang et al. (2023), mediante inmunocitoquímica, confirmaron la presencia de TMEM249 o CatSper theta (CatSper θ) en la pieza principal del flagelo en espermatozoides epididimarios. CatSper θ es una subunidad con cuatro nanodominios lineales. Su papel se atribuye a participar como andamiaje para la subunidad CatSper4 (formadora de poros) y el ensamblaje del complejo CatSper (Huang et al., 2023).
La ausencia de CatSper θ indica inactividad de CatSper pero no afecta la expresión de las otras subunidades del canal. Así mismo, la generación de ratón KO CatSper θ no presentó diferencias en el número y morfología de los espermatozoides epididimarios. Sin embargo, no hubo camada, debido a la incapacidad de los espermatozoides para fecundar los ovocitos. Por lo tanto, la ausencia de CatSper θ afecta el desarrollo de la movilidad hiperactivada, causando infertilidad (Huang et al., 2023).
Por otra parte, de acuerdo con la expresión de ARNm de los genes de CatSper, Tmem249 se expresa en el testículo. Además, determinaron a través de estudios de cribado genómico que el gen Tmem249 exhibe coevolución genómica con los genes de las subunidades Catsper1-4, Catsper β-δ y EFCAB9 (Huang et al., 2023).
Distribución filogenética
En los estudios de genómica comparativa y filogenia utilizaron búsquedas BlastP, consistente en comparar la secuencia de aminoácidos contra secuencias almacenadas en estas bases de datos, y TBlastn para comparar una secuencia de proteína con una base de datos de nucleótidos (Cai & Clapham, 2008; Cai, Wang & Clapham, 2014); reportan que el canal CatSper se conserva evolutivamente en el genoma de varios organismos, en los que está amplia pero heterogéneamente distribuido en todos los linajes de eucariotas, desde mamíferos y reptiles hasta invertebrados como equinodermos, cnidarios y ctenóforos (Figura 3). Sin embargo, los genes CatSper se pierden en los gusanos redondos, los insectos, los peces, los teleósteos, los anfibios y las aves (Figura 4), (Cai & Clapham, 2008; Cai, Wang & Clapham, 2014; Romero & Nishigaki, 2019). En estos estudios, para determinar qué especies conservan CatSper, consideraron que deben tener al menos las cuatro subunidades α formadoras de poros y utilizaron secuencias de proteínas de diferentes especies, para la consulta en las bases de datos genómicas como la del Centro Nacional de Información Biotecnológica (NCBI, por sus siglas en inglés), Genómica y Genoma de Ensembl (Romero & Nishigaki, 2019).
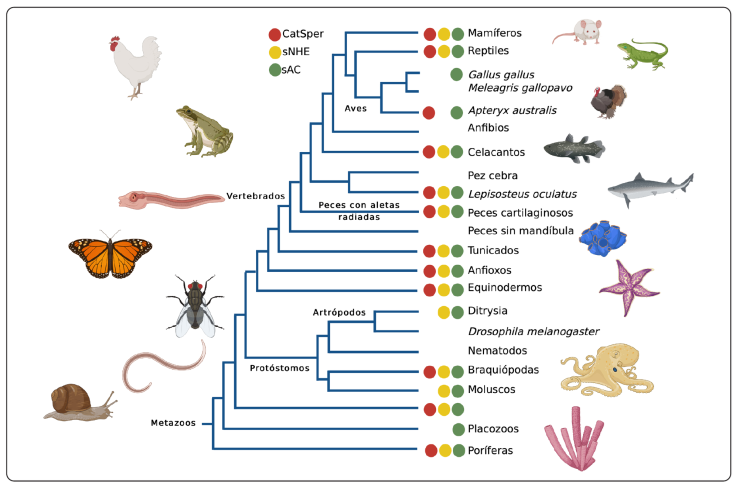
Modificado de: Romero & Nishigaki, 2019.
Figura 3 Distribución filogenética de CatSper, sNHE y sAC en mamíferos, reptiles, aves, peces, artrópodos y protóstomos. Cada círculo de color representa la presencia de la proteína: rojo-CatSper, amarillo-sNHE y verde-sAC.
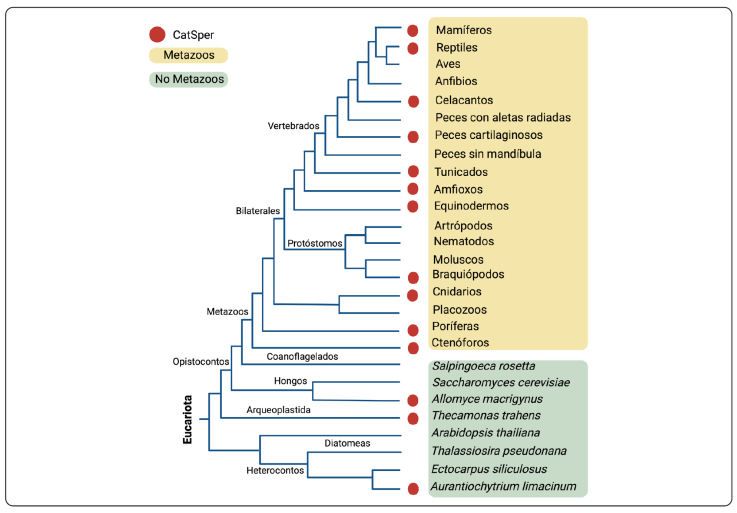
Modificado de: Romero & Nishigaki, 2019.
Figura 4 Distribución genética del canal CatSper entre los grupos taxonómicos de metazoos (amarillo) y de especies no metazoarias (verde).
Cai & Clapham (2008) informan de un pseudogén Catsper. En otras palabras, el gen que codifica a CatSper ha sido inactivado durante la evolución debido a mutaciones en su secuencia, lo que ha provocado su pérdida en varias especies. La divergencia entre CatSper1-4 sugiere que las variantes evolutivas se han adquirido a través de restricciones funcionales alteradas después de la replicación ancestral.
La distribución filogenética de CatSper se ha correlacionado con otras proteínas involucradas en la movilidad espermática como: El intercambiador Na+/H+ específico del espermatozoide (sNHE), proteína transmembranal encargada de regular el pH intracelular (pHi), (Wang, King, Quill, Doolittle & Garbers, 2003); el adenilato ciclasa soluble (ACs), es el responsable de la síntesis del monofosfato de la adenosina cíclico (AMPc) y la activación de la proteína quinasa A (PKA), (Xie et al., 2006). Al reportar que las especies de metazoos que conservan CatSper también conservan sNHE y ACs, sugieren una coevolución entre las tres proteínas (Figura 3).
Activación
Se ha informado que CatSper está moderado débilmente por el voltaje, la alcalinización intracelular, moléculas presentes en el tracto reproductivo femenino y las vías de señalización que incluyen cAMP/PKA (Kirichok, Navarro & Clapham, 2006; Lishko, Botchkina, Fedorenko & Kirichok, 2011; Orta, de la Vega, Martín-Hidalgo, Santi, Visconti & Darszon, 2018; Strünker et al., 2011), e indirectamente por hormonas como la progesterona y las prostaglandinas. Además, hay informes que indican que CatSper sirve como un sensor polimodal para algunas sustancias químicas que ayudan a los espermatozoides durante su ruta a través del tracto femenino (Brenker et al., 2012).
Voltaje
CatSper es un canal débil que depende del voltaje. Es decir, su sensibilidad al voltaje regula la actividad del canal, como lo demuestra la electrofisiología, donde la activación de la corriente de CatSper es débil en comparación con canales iónicos de Ca2+ (CaV) fuertemente sensibles al voltaje (Kirichok et al., 2006).
Progesterona
Se ha descubierto que CatSper puede ser estimulado por las hormonas esteroides, la más estudiada es la progesterona (P4) (Lishko et al., 2011; Strünker et al., 2011). Los espermatozoides depositados en el tracto reproductivo femenino están expuestos a P4, que es sintetizada y liberada por las células del cúmulo que rodean al ovocito (Brown et al., 2017). Se ha demostrado que P4 induce un aumento de [Ca2+]i en los espermatozoides de ratón (Romarowski et al., 2016) y de humanos (Brown et al., 2017), al desencadenar respuestas fisiológicas como la movilidad hiperactivada (Achikanu, Pendekanti, Teague & Publicover, 2018), quimiotaxis (Oren-Benaroya, Orvieto, Gakamsky, Pinchasov & Eisanbach, 2008) y RA (Romarowski et al., 2016).
El aumento espacio-temporal de [Ca2+]i en el espermatozoide promovido por P4 ocurre desde el flagelo hasta la cabeza en cinco patrones diferentes: gradual, oscilatorio, transitorio tardío, transitorio inmediato y sostenido (Romarowski et al., 2016). Lishko et al. (2011), determinaron mediante patch-clamp que P 4 activa el canal CatSper en espermatozoides de humanos y observaron que la amplitud de la corriente monovalente del canal aumenta a concentraciones nanomolares de P4. A diferencia de los espermatozoides de ratón, la sensibilidad a P4 es reducida, ya que sólo se activa a concentraciones de 50-100 µM (Lishko et al., 2011; Romarowski et al., 2016). Sin embargo, la concentración de P 4 necesaria para estimular la capacitación y/o RA varía según la especie, generalmente se encuentra en el rango micromolar (Gatica et al., 2013). Recientemente, Mendoza-Sánchez et al. (2023) describieron que en los Chiroptera (murciélagos) las concentraciones nanomolares de P4 activan CatSper, semejante a la respuesta de los espermatozoides de humanos.
Los investigadores mencionan que la señalización de las hormonas esteroides en las células somáticas depende de que los receptores nucleares desencadenen una respuesta genómica. Sin embargo, al no tener una actividad transcripcional, sugieren que los espermatozoides responden a P4 por una vía no genómica a través de receptores en la membrana plasmática. También creen que la activación de CatSper sucede por la unión directa de P4 al canal, o por la unión de P4 a una hidrolasa de serina ABHD2 (dominio hidrolasa α/β, proteína 2; 425 aminoácidos) expresada en los espermatozoides. Se determinó la presencia de un endocannabinoide 2-araquidonoilglicerol (2-AG) en la membrana plasmática del espermatozoide, que se sintetiza a partir del ácido araquidónico y glicerol por medio de la enzima diacilglicerol lipasa. El 2-AG tiene una función desconocida en los espermatozoides, en el tracto reproductor masculino y en el femenino. Sin embargo, se atribuye como inhibidor endógeno del canal CatSper; proponen que la unión de P4 con ABHD2 es causa de la degradación por hidrólisis de 2-AG, lo que activa el canal y permite el flujo de Ca2+ hacia el espermatozoide (Figura 5), (Miller et al., 2016).
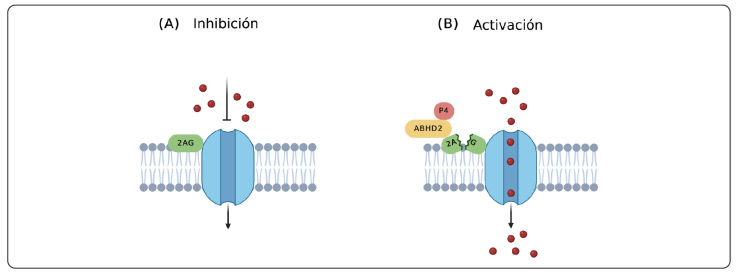
Figura 5 Estimulación del canal CatSper por progesterona. (A) Inhibición de CatSper por el endocannabinoide 2-araquidonoilglicerol (2-AG). (B) Es posible que la activación del canal sea estimulada por la unión de P4 a través de una proteína α/β hidrolasa del dominio serina, proteína 2 (ABHD2), lo que promueve la degradación de 2-AG producido en la membrana plasmática del espermatozoide, activa el canal y permite así la entrada de Ca2+ al interior del espermatozoide (Miller et al., 2016).
Alcalinización
En los mamíferos, los espermatozoides almacenados en el epidídimo se encuentran en un medio intracelular y extracelular con un pH ácido, condición fisiológica que los mantiene en estado de quiescencia, pero en el tracto reproductivo femenino el pH se torna más alcalino hacia el oviducto (Liu, Wang & Chen, 2012). El aumento del pHi en los espermatozoides es esencial para la hiperactivación y la RA (Achikanu et al., 2018; Chávez et al., 2017). Se ha reportado que el pHi regula la movilidad y el influjo de Ca2+ al activar CatSper en espermatozoides de ratones y humanos (Kirichok et al., 2006; Lishko et al., 2011; Strünker et al., 2011). El análisis electrofisiológico en espermatozoides indica que las corrientes de CatSper se potencian por la alcalinización intracelular al permitir la entrada de Ca2+ al citosol (Strünker et al., 2011).
En los espermatozoides, el cloruro de amonio (NH4Cl) se ha utilizado para alcalinizar el citosol, con esto se induce un aumento de [Ca2+]i sin desencadenar la liberación de Ca2+ de los depósitos internos y la reacción acrosómica en los espermatozoides de ratón y en los humanos, por lo tanto, esta base débil se ha utilizado durante el estudio del flujo de Ca2+ durante la capacitación espermática (Chávez et al., 2017; Orta et al., 2018). El mecanismo de activación de CatSper por alcalinización se debe a que el extremo amino terminal de la subunidad α-CatSper1 es rico en histidina, que tiene un papel importante en la detección de pHi (Kirichok et al., 2006; Ren et al., 2001). Además, la actividad de CatSper está asociada a diferentes canales iónicos que participan en la regulación de pHi, incluyendo el canal de protones Hv1 (Lishko et al., 2010).
AMPc/PKA
Entre los cambios que ocurren durante la capacitación espermática se encuentra un aumento en la concentración intracelular de bicarbonato (HCO3-), (Puga Molina, Luque, Balestrini, Marín-Briggiler, Romarowski & Buffone, 2018). El HCO3 - estimula el adenilato ciclasa atípica (Adcy10), que aumenta los niveles de la adenosina monofosfato cíclico (AMPc) y que activa la PKA (Brenker et al., 2012). Sin embargo, existe controversia sobre si CatSper está regulada por la vía de señalización que incluye el aumento de AMPc y la activación de PKA. Orta et al. (2018) demostraron mediante el uso de activadores de PKA como 8- Br-AMPc (análogo de AMPc), inhibidores como PKI y H89, y HCO3-, que la respuesta [Ca 2+]i dependiente de CatSper está regulada por la actividad de PKA. Es decir, la elevación de AMPc intracelular facilita la entrada de Ca2+ vía CatSper a través de la fosforilación dependiente de PKA. Además, se observó en registros electrofisiológicos que la adición de AMPc en los espermatozoides de ratón activa claramente la corriente CatSper y es inhibida por PKI y H89. Por lo tanto, se sugiere que la actividad de CatSper está regulada por la activación de la vía AMPc/PKA (Orta et al., 2018).
Sin embargo, Wang et al. (2020), demostraron mediante registros electrofisiológicos que en humanos el canal CatSper no es activado por AMPc directa o indirectamente a través de la vía AMPc/PKA. Sin embargo, concentraciones no fisiológicas de AMPc y análogos de este nucleótido cíclico (8-Br-cAMP), activan a CatSper desde el exterior a través de un sitio de unión desconocido diferente al de los esteroides. También se demostró que la respuesta de entrada de Ca2+ que causa HCO3-es causada por la alcalinización intracelular descontrolada de los tampones con HCO3- (que activa a CatSper), y no por su relación con la vía AMPc/PKA como se consideró previamente (Wang et al., 2020). Además, se demostró que los inhibidores de PKA se basan en la interacción directa con CatSper y no en la inhibición de PKA, ya que se encontró que la respuesta provocada por estos fármacos se eliminaba en ausencia de CatSper (Wang et al., 2020).
Inhibición farmacológica
Durante el estudio de la función de CatSper, se han utilizado varios fármacos que suprimen su actividad, como es el caso del NNC55-0396, que inhibe su corriente eléctrica activada por P4 en los espermatozoides de ratón (Lishko et al., 2011) y la señal de Ca2+ inducida por alcalinización utilizando NH4Cl en espermatozoides de humanos (Strünker et al., 2011). Aunque el NNC55- 0396 fue descrito como un inhibidor de los canales de Ca2+ de tipo T, su afinidad por CatSper es al menos diez veces mayor a la de los canales tipo T (Huang et al., 2004; Lishko et al., 2011). Por otro lado, se han probado varios inhibidores del canal Ca V que suprimen la respuesta de Ca2+, como la Nifedipina, el Verapamilo, el Diltiazem, el Níquel y el Mibefradil. Sin embargo, sólo el Mibefradil inhibe significativamente la respuesta de Ca2+ (Strünker et al., 2011), así como MDL12330A suprime la respuesta estimulada por la alcalinización y P4 en el espermatozoide de humanos (Brenker et al., 2012).
En el año 2018, se informó que el compuesto RU1968 suprimía la señalización de Ca2+ al inhibir CatSper en los espermatozoides humanos, en los de ratón y en los de erizo de mar mediante un mecanismo no descrito. El compuesto no muestra efectos tóxicos en los espermatozoides, ni afecta la actividad de otros canales como SLO3 en espermatozoides de ratón y de humanos (Rennhack et al., 2018). Además, en los espermatozoides humanos, RU1968 suprimió la respuesta de movilidad provocada por P4 y abolió la de quimiotaxis mediada por CatSper en los espermatozoides de erizo de mar (Rennhack et al., 2018; Torrezan-Nitao, Brown, Mata-Martínez, Treviño, Barratt & Publicover, 2021).
Conclusiones
El canal CatSper regula la entrada de Ca2+ en los espermatozoides necesaria para la movilidad hiperactivada. Este canal es un complejo formado por al menos 10 subunidades. Se ha demostrado que la ausencia de alguna de las subunidades afecta la actividad del canal de forma parcial o total, perjudicando la fertilidad masculina. Además, el análisis bioinformático sugiere una distribución heterogénea del canal y sus subunidades entre los grupos taxonómicos. También, diversos estudios muestran que la actividad de CatSper está regulada por diversos mecanismos que han dilucidado la función y/o participación del canal en los diferentes procesos fisiológicos de los espermatozoides.
En el futuro, investigaciones comparativas de CatSper en diversas especies de mamíferos y otros taxones contribuirán a esclarecer los mecanismos de activación y regulación de este canal, al proporcionar información valiosa sobre su evolución y diversidad funcional. Estos avances también ofrecen oportunidades para desarrollar anticonceptivos masculinos no hormonales, específicos y seguros, basados en la modulación del canal lo que representaría un hito en la salud reproductiva masculina.










 nueva página del texto (beta)
nueva página del texto (beta)